セカンドオピニオンから ペットロスまで どうぶつよろず相談
院長のコラム 2020年2月20日
『イヌと筋ジストロフィー⑤ 分子レベルでの治療Ⅱ』
 |
 |
|
イヌと筋ジストロフィー⑤ 分子レベルでの治療Ⅱ |
||
2020年2月20日 皆様、KVC Tokyo 院長 藤野 健です。 筋ジストロフィーのお話の第5回目です。 以下、本コラム作成の為の参考サイト:https://www.colliehealth.org/degenerative-myelopathy/American College of Veterinary Internal Medicinehttps://www.acvim.org/Muscular Dystrophy in Dogshttps://wagwalking.com/condition/muscular-dystrophyhttps://geneticliteracyproject.org/2018/10/25/promising-treatment-for-duchenne-muscular-dystrophy-developed-with-crispr-gene-editing/https://en.wikipedia.org/wiki/Muscular_dystrophyhttps://ja.wikipedia.org/wiki/筋ジストロフィー一般社団法人 日本筋ジストロフィー協会https://www.jmda.or.jp/デュシェンヌ型筋ジストロフィー(Duchenne muscular dystrophy:DMD)https://www.jmda.or.jp/mddictsm/mddictsm2/mddictsm2-1/mddictsm2-1-1/https://www.mda.org/disease/duchenne-muscular-dystrophyhttps://ja.wikipedia.org/wiki/福山型先天性筋ジストロフィー神戸大、筋ジストロフィー「福山型」治療に道2011/10/6付 日本経済新聞https://www.nikkei.com/article/DGXNASDG0502M_V01C11A0CR8000/?at=DGXZZO0195591008122009000000https://ja.wikipedia.org/wiki/ジストロフィンhttps://ja.wikipedia.org/wiki/フクチンhttps://science.sciencemag.org/content/362/6410/86https://geneticliteracyproject.org/2018/10/25/promising-treatment-for-duchenne-muscular-dystrophy-developed-with-crispr-gene-editing/https://www.actionduchenne.org/what-is-duchenne/duchenne-explained/glossary-of-research-terms/stop-codon-readthrough/国立研究開発法人 国立精神・神経医療研究センター 神経研究所 遺伝子疾患治療研究部https://www.ncnp.go.jp/nin/guide/r_dna2/en/research_dystrophy.htmlGENEReviews Japan 拡張型心筋症概説(Dilated Cardiomyopathy Overview) http://grj.umin.jp/grj/dcm-ov.htm筋収縮を調整する分子機構https://www.jst.go.jp/pr/announce/20030703/01.html京都大学循環器内科 カルシウム拮抗薬http://kyoto-u-cardio.jp/shinryo/chiryo/00607/0060706/iPS細胞を使った遺伝子修復に成功 -デュシェンヌ型筋ジストロフィーの変異遺伝子を修復-2014年11月27日http://www.kyoto-u.ac.jp/ja/research/research_results/2014/141127_1.htmlhttps://ja.wikipedia.org/wiki/核酸医薬 |
||
 |
 |
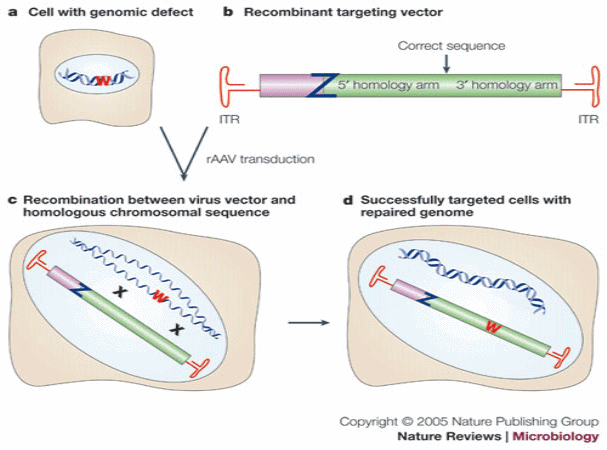
Gene targeting with recombinant adenoviral vectors
https://www.nature.com/wls/content/gene-targeting-with-recombinant-adenoviral-vectors-22302/
ウイルス感染により遺伝子を導入する方法を示す簡略な図説
アデノウイルスに正常な遺伝子の断片を組み込み(b)、それを異常細胞 (a)に感染
させます(c)。すると、遺伝子の異常部分Wと正常な部分が交換(=組み替え)さ
れ正常な遺伝子を持つ細胞に戻ります(d)。
 |
 |
|
前回ご紹介した論文Journal of Muscle Research and Cell MotilityJune 2019, Volume 40, Issue 2, pp 141-150 First Online: 09July 2019https://link.springer.com/article/10.1007%2Fs10974-019-09535-9What is the level of dystrophin expression required for effective therapy of Duchenne muscular dystrophy? (アブストラクトのみ無料)Dominic J. WellsNeuromuscular Diseases Group, Department of Comparative Biomedical Sciences Royal Veterinary College LondonUK ここに、以下の研究手法が採り上げられています。これについて簡略に順に解説していきます。全て遺伝子絡みの手法となります。 ① viral vector mediated delivery of a recombinant dystrophin gene② antisense oligonucleotide mediated exon-skipping to restore the open reading frame in the dystrophin mRNA③ read-through of premature stop mutations④ genome modification using CRISPR-Cas9⑤ cell based transfer of a functional dystrophin gene.今回はこの内の、①、②までを扱います。 ① viral vector mediated delivery of a recombinant dystrophin gene組み替えジストロフィン遺伝子の、ウイルスベクターを媒介しての導入 正しいジストロフィンン遺伝子を準備してその部分をカットし、それをウイルスに組み込んで目的とする筋細胞に感染させ(病気を起こさないウイルスを利用)、核内にその遺伝子を入れるとの方法です。最近の手法では、その遺伝子は染色体に組み込まれることなく機能を発現しますので、子孫に遺伝して伝わったり発癌の原因になったりするおそれがありません。但し、ジストロフィンタンパク質は巨大ですのでその設計図となる遺伝子部分も巨大サイズとなり、ウイルスに組み込んで運搬するのが困難です。そこでジストロフィン遺伝子の必要不可欠な部分だけを使うことを考え、短縮型の遺伝子を作出(国立精神・神経センター神経研究所所長 武田伸一氏が開発)しそれを導入したところ、ジストロフィンとして機能することが世界で最初に確認できました。 詳細は、https://www.jmda.or.jp/mddictsm/mddictsm6/mddictsm6-1/ をご参照下さい。問題はそのウイルスを如何に効率よく筋細胞に感染させるかですが、現在は筋内に注入するとの手法が検討されているようですね。筋肉はマスが大きく、全身の筋の筋細胞に感染を起こす量の大量のウイルスをどうやって体内或いは筋中ににバラ撒くかですが、免疫が作動してウイルスを退治する状況に陥らせるのも困ります。一時的に免疫抑制状態にさせた上で強力な感染を生じさせるのかなどと門外漢の院長は想像をたくましくさせています。その後に自然免疫が発動して用済みのウィルスを始末する作戦ですね。 |
||
 |
 |
Figure 1- available via license:
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International
https://www.researchgate.net/figure/Antisense-mediated-exon-skipping-rationale
-for-Duchenne-muscular-dystrophy-DMD-a_fig6_221851227
Engineering Multiple U7snRNA Constructs to Induce Single and Multiexon-skipping
for Duchenne Muscular Dystrophy, Goyenvalle A. et al.
Molecular Therapy 20 (6):1212-21 ・ February 2012 DOI: 10.1038/mt.2012.26
(無料で全文読めます)
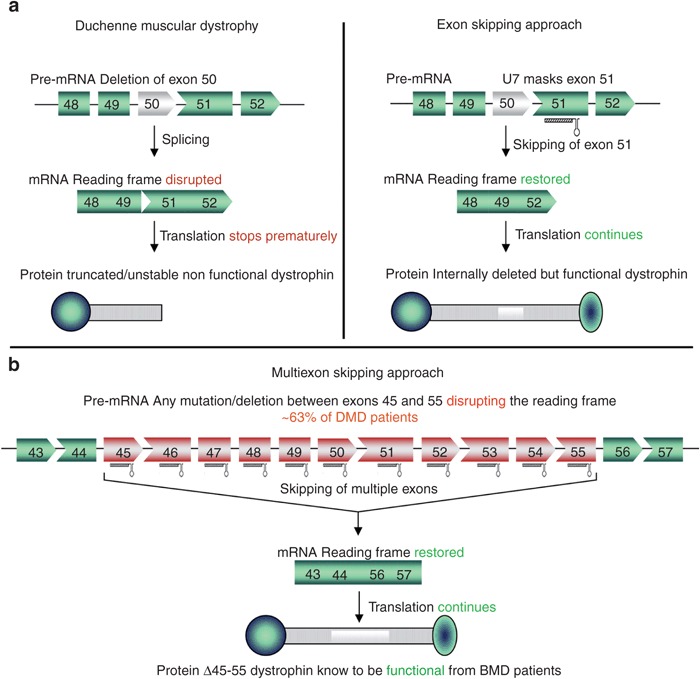
エクソンスキップ法
DMD患者の一部はジストロフィン前駆 mRNA の正しい書き出しを途中でズレさせる遺伝
変異を持って居ますが (a左)、出来たジストロフィン(マッチ棒の様なもの)は不完全で機
能しません。その不具合を読み飛ばしてジストロフィンを作らせるようにします (エクソンス
キップ法)。出来たものは少し短いジストロフィンですが正常に機能します(a右)。エクソン
45から 55迄に存在する異常に対しては丸ごとその区間を読み飛ばしてジストロフィンを
作る手もありますが、その短いジストロフィンはベッカー型筋ジストロフィーBMDの持つジ
ストロフィンと同じ物となり、DMD患者の最大 63%が症状が解消あるいは改善される可
能性があります(b)。
異常なエクソンごとに対応して核酸医薬をオーダーメードで作るのではなく、多くの患者が
異常を抱える遺伝子部位を丸ごと飛ばし読みする薬を作り多くの者に投与すると合理的と
の考えです。7年前の論文ですが、先験的なアイデアと感心させられます。
 |
 |
|
② antisense oligonucleotide mediated exon-skipping to restore t he open reading frame in the dystrophin mRNAジストロフィンメーセンジャーRNAを正しく読み込ませる為の、アンチセンスオリゴ核酸を用いたエクソンスキップ法 この方法の具体例として以下引用します: 「https://www.ncnp.go.jp/press/release.html?no=502令和元年11月6日国立研究開発法人 国立精神・神経医療研究センター(NCNP)デュシェンヌ型筋ジストロフィー治療薬(NS-089/NCNP-02)の医師主導治験(First In Human試験)開始について国立研究開発法人 国立精神・神経医療研究センター(小平市 理事長:水澤英洋、以下、NCNP)は、日本新薬株式会社(本社:京都市、社長:前川重信、以下、日本新薬)と共同研究を進めてきたアンチセンス核酸医薬品であるデュシェンヌ型筋ジストロフィー(以下、DMD)治療薬(NS-089/NCNP-02)を用いて、医師主導治験(First In Human試験)を本日11月6日より開始いたします。<開発の背景>デュシェンヌ型筋ジストロフィー(DMD)は、ジストロフィン遺伝子の変異が原因で、筋の細胞膜からジストロフィン・タンパク質が失われ、徐々に筋力低下が進む難病で、男児に発症します。「エクソン・スキップ治療」は、アンチセンス核酸と呼ばれる短いDNAの様な合成核酸を用いて、メッセンジャーRNA前駆体から成熟メッセンジャーRNAが作られる過程で、タンパク質に翻訳されるエクソン領域の一部を人為的に取り除く(スキップする)ことで、アミノ酸読み取り枠のずれを修正する治療法です(イン・フレーム化といいます)。この結果、正常なジストロフィンに比べると、タンパク質の一部が短縮するものの、機能を保ったジストロフィンが発現して筋機能の改善が期待できます。この治療でスキップの対象となるエクソンは患者の変異形式に応じて異なり、現在までに、本邦では、エクソン53スキップ薬であるNS-065/NCNP-01(ビルトラルセン)が承認審査中です。しかしながら、エクソン53スキップ薬が適応にならない患者に対して、別のエクソンを標的とした薬剤の開発が喫緊の課題となっています。<開発の内容>NS-089/NCNP-02は、NCNPと日本新薬が共同で開発した世界初のエクソン 44 スキップ薬です。モルフォリノ核酸が本来有する高い安全性に加えて、特許出願技術である新規高活性配列探索法を用いて開発した配列連結型のモルフォリノ核酸製剤であり、高いエクソン・スキップ活性を有しています。これまでに得られた非臨床試験の結果からは、エクソン44スキップに応答する変異形式の DMD患者細胞における有効性が確認されており、病気の進行を抑えることが期待されます。<今後の展開>本試験は、国産アンチセンス核酸医薬品であるNS-089/NCNP-02を、ヒトに対して初めて投与する医師主導治験であり、NCNP病院において6例のDMD患者さんに対して行われます。主要評価項目である安全性の他、NS-089/NCNP-02投与後の薬物動態、ジストロフィン・タンパク質の発現確認等の有効性についても検討を行う予定です。 患者さんはジストロフィン遺伝子を持ってはいても、その遺伝子の中に、遺伝子を読み込む場所をズレさせるような間違った部分が挟み込まれている場合があります。エクソンスキップ法とは、薬剤を投与することで、その様なジストロフィン設計図の誤った記述部分を飛ばして(スキップして)ジストロフィンを作出させる方法です。タンパク質が合成される過程では、DNAの遺伝子暗号部分を mRNA(メッセンジャーRNA)が一度転写し、それを元にタンパク質が合成されますが、その途中の過程で修整を加えようとの発想ですね。昔のレコード盤を作製する時に、まずラッカー原盤に針で溝を刻ませ、次いでそれをメッキして雌型を作り、その雌型を元にして大量の市販レコードを作っていましたが、原版のキズのついた箇所 (これは手を触れない)を、雌型の段階で修整してから大量のレコードをスタンピングする様な遣り方ですね。この様な目的の薬剤を核酸医薬と呼称します。異常な遺伝子そのものを治すのでは無く、そこからタンパク質が合成される途中の過程に介入する作戦ですね。既に上記の治験が6名の患者さんに対して実施とのアナウンスですが首尾良く進む事を祈っています。 尚、アンチセンスオリゴヌクレオチド (ASO)を含めた核酸医薬品については https://ja.wikipedia.org/wiki/核酸医薬 に詳述されています。 投与形態、即ち、点滴で血中に投与するのか、飲み薬の形態か、などは上記説明文からは情報が得られません。 |
||
 |
 |