�Z�J���h�I�s�j�I������ �y�b�g���X�܂Ł@�ǂ��Ԃ�낸���k
�@���̃R���� �Q�O�P�X�N�W���P��
�w�]�E�͊��ɂȂ�ɂ����H�@�]���r��`�qLIF�̓����A�x
 |
 |
|
�]�E�͊��ɂȂ�ɂ����H�@�]���r��`�qLIF�̓����A |
||
�Q�O�P�X�N�W���P�� �F�l�AKVC Tokyo �@���@����@���ł��B �@�O��ɑ����ȉ��̘_���̏Љ�ł��B �@Cell Rep. 2018 Aug 14; 24(7): 1765-1776 A Zombie LIF Gene in Elephants Is Upregulated by TP53 to Induce Apoptosis in Response to DNA Damage.�u�]�E�̃]���r��`�q LIF �� TP53 �ɂ�蘴�i����ADNA �����ɔ������A�|�g�[�V�X��U������vVazquez JM, Sulak M, Chigurupati S, Lynch VJ .�i�����őS�������邱�Ƃ��ł��܂��j ���^����https://www.ncbi.nlm.nih.gov/pubmed/30110634AbstractLarge-bodied organisms have more cells that can potentially turn cancerous than small-bodied organisms, imposing an increased risk of developing cancer. This expectation predicts a positive correlation between body size and cancer risk; however, there is no correlation between body size and cancer risk across species ("Peto's paradox"). Here, we show that elephants and their extinct relatives (proboscideans) may have resolved Peto's paradox in part through refunctionalizing a leukemia inhibitory factor pseudogene (LIF6) with pro-apoptotic functions. LIF6 is transcriptionally upregulated by TP53 in response to DNA damage and translocates to the mitochondria where it induces apoptosis. Phylogenetic analyses of living and extinct proboscidean LIF6 genes indicates that its TP53 response element evolved coincident with the evolution of large body sizes in the proboscidean stem lineage. These results suggest that refunctionalizing of a pro-apoptotic LIF pseudogene may have been permissive (although not sufficient) for the evolution of large body sizes in proboscideans.Copyright 2018 The Author(s). Published by Elsevier Inc. All rights reserved.PMID: 30110634DOI: 10.1016/j.celrep.2018.07.042�ȉ��A�{�R�����쐬�̂��߂̎Q�l�T�C�ghttps://ja.wikipedia.org/wiki/�~�g�R���h���Ahttps://ja.wikipedia.org/wiki/�A�|�g�[�V�X�ȉ����p�F�uDNA�����Ȃ� �� p53 �� �~�g�R���h���A���Bax�ABak �Ȃǂ̃^���p�N������Ȃ�V�O�i���n�ɂ�鐧��i�܂��̓~�g�R���h���A���ُ̂̈�j �� �~�g�R���h���A����V�g�N����c�̘R�o �� �J�X�p�[�[-9 �� �J�X�p�[�[-3�@�i�r�����j �J�X�p�[�[-3�����̑��̃^���p�N��������Ȃǂ��ăA�|�g�[�V�X�����s������B�vWikipedia contributors. "�A�|�g�[�V�X." Wikipedia. Wikipedia, 22 Feb. 2019. Web. 22 Feb. 2019.���A�|�g�[�V�X�Ƃ́A���̑�������̕s�v�ȁA�����͊��������זE��j��@�\�ł����A���T�R��`�q�����������A���ꂪ�~�g�R���h���A��s���艻�����ăV�g�N���E���b��R�o�����A���ꂪ�X�ɃJ�X�p�[�[�n�i�����ă^���p�N����Ȃ�זE�\���̉��䍜���̂��̂�j��d�g�݂ł��ˁB���~�g�R���h���A���֗^���Ȃ����[�g�̃A�|�g�[�V�X������܂��B |
||
 |
 |
 |
 |
|
�@���āA����Љ�܂����_���̋����҂ɁA�ȑO�̃R�����A�Ȃ��]�E�͊��ɂȂ�Ȃ̂��A�̒��ŏЉ�� Lynch ����������Ă��܂��̂ŁA�ނ̌����O���[�v��������o�����ƌ�����ł��B�����͋@�֏e�̒e�ۂ�ł��̂悤�ɁA����ł�������܂ł��Ɨ��咣����_���ŁA�\���I�ɂ��ǂ݂₷���p���Ƃ͂ƂĂ������Ȃ��Ǝv���܂����A�O�O�ɓǂݐi�߂�ƁA�����������Ƃ�����ɑN���ɗ����ł���l�ɂȂ�܂��B �@�U��`�q �i�����łj�̓W�����N�̈�`�q�ŁA�{���A��`�q�͂܂Ƃ��ɋ@�\����ƃ^���p�N�����������A���̃^���p�N�����l�X�Ȑ��̒����Ɋ֗^���Đg�̂����N�ɕۂ̂ł����A�U��`�q�Ƃ͂��̃^���p�N�������\�������A��������ߍ���ŋ���l�ȑ����ł��B����Δ�������ł���݂����ȑ��݂������̂ł����A���ꂪ���̈�`�q�̈ꕔ����ς��邱�Ƃ� LIF �i�����a�j�~���q�ƌĂ�邪�l�X�ȋ@�\�������A�זE�̔j��@�\�����̂P�j �̂U�� �iLIF6�j ���Y���\�Ȉ�`�q�Ƃ��ĕ����𐋂��ALIF6�� DNA�����������זE�����Ȕj��ɓ����@�\�����䂦�A�����O��Ƃ��Ă���ȍ~�]�E�̑�^���������ꂽ�A�Ƃ̓��e�ł��BLIF ���Y���\�Ȉ�`�q�� �T�X�O�O���N�O ���疰���U��`�q�Ƃ��ă]�E�̑c�悪�����Ă����̂ł����A���݂̑�^�̃]�E�ɘA�Ȃ�i���̊����o�������̂� �Q�X�O�O���N�O �䂦�A���̍���LIF6 ���Y���\�Ȉ�`�q�Ƃ��ĕ����𐋂����̂��낤�ƒ��ғ��͐��_���܂��B�܂��A���������R�O�O�O���N�����Ă�����ł��ˁB �@DNA �̒��ɖ��ʂȔz�ʂ�����Ȃǂƌ����܂����A���݂͒��s����Ԃł��A�O�N�i�O�疜�N�H�j�Q���Y�ł͂���܂��A�����������Ė𗧂��Ƃ����ۂ����Ƃ̘b�ł��B���ɗ����Ă��Ȃ�����ƃ]�E�̈�`�q�����ɍ킬���Ƃ���ċ����̂Ȃ�A�]�E�͏������܂܂ɗ��܂�A�o�N�݂����Ȑ������̂܂܂�������������܂���B�����͑��Ƃ̋����ɔs���ł��Ă������B �@�Z���Ԃł̐��ю�`�A������`�I�Ȍ����̕����ɑ��A��`�q���g�����̐\�����l�ɂ������܂��B���݂̎Љ�E�o�Ϗ�ɓK�����A�����ӎ������A���̐����w�͉Ƃł���A�X�ɂ͎��͂̐l�S����������ɓK�����҂���Ƃ̎В��ɏA���A����A�ǂ��������̍˔\����肭�����ł��Ȃ��Ȃ��Ɗ�����҂����ۋ����ł����A�В��ɂ��Ă��q�g�Ƃ��Ă̈�`�q�̂����ꕔ�̕���������ɉ����Ď��������o���Ă���ɉ߂����A���̕����̎��͂ǂ���������܂���B��ʂ̋��҂ɉ߂��Ȃ��҂����O�͖��ɗ����Ȃ��Ƒ���r�����鐢�̒��́A��`�q��������������ϓ_���炵�Ă�����Ȃ̂ł��傤�B�����������͓�{�̑����g���ē����A�����͂��̏�ɓ��݂Ƃǂ܂�A���̎d�蒼��������݂̂ł��B���ɂ́A���g�̃]���r��`�q�i����j�����̐�̎q���ŊJ�Ԃ���\��������܂��̂ŁA�A�ؓ��̖��ӔC�V���[�Y�̂��Ƃ��A���Ƃ̂��Ƃ͔C������ƁA�^����ꂽ���ɂĐl�����y��������̂���ł��ˁB |
||
 |
 |
https://youtu.be/dDbRkSEOajc
�j�b�|�����ӔC��Y 1962�N�ABlues Harp 2012/10/01 �Ɍ��J�B
�]���r��`�q�Ȃ�ʖ��ӔC��`�q�������Ă���̂����B
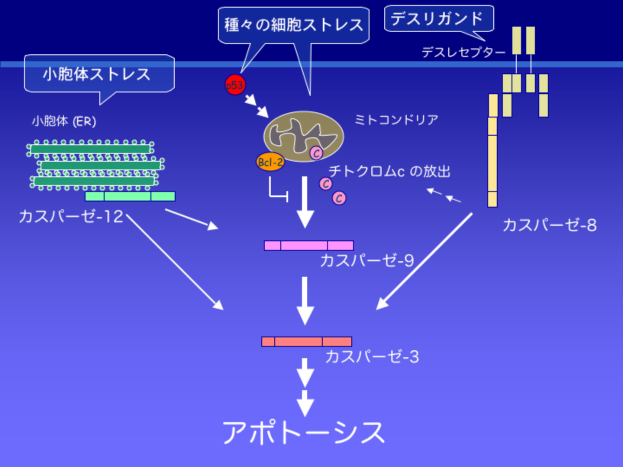
�A�|�g�[�V�X�̌o�H�i�J�X�p�[�[�ˑ��o�H�j�@credit: �Q�O�O�T�N Y tambe ��
https://ja.wikipedia.org/wiki/�t�@�C��:Apoptosis_scheme.png
���ϖ����B���C�Z���X���͏�L url �Ɋ܂܂�܂��B
��̃C���X�g�ŁAp53 ��`�q�i�����ȐԊہj�ƃ~�g�R���h���A�̊Ԃ� LIF6 ����݂��鎖��
���炩�ɂȂ�����ł��ˁB�~�g�R���h���A�͊e�זE�����萔�S�`������݂��܂�
�̂ŁA�������� ���T�R��`�q�̐����������������ǂ��~�g�R���h�A��j��ł��A���ʂ�
���čזE�����Ղ��Ȃ邱�Ƃ͗����ł��܂��B
 |
 |
|
�@�R��ᇈ�`�q �o�T�R �̐��������������ł͖����A�s�o�R�T �ɋ��肨�O�����Ǝw�߂����@LIF6 �Y����`�q���o�� �iLIF6 �͒��ڂɍזE�ċz�̃J�i���ƂȂ�~�g�R���h���A��j�A�זE�����N�����j �������ƂŁA�c�m�` �����������זE�ɑ��Ă�������͂Ɏ��Ȕj��\�ƂȂ����A����Ń]�E�����Ɋ��������邱�Ƃ������A�ڏo�x���傫���Ȃꂽ�̂��A�ƁA�X�Ɉ�����ݍ��𖾂��Ȃ��ꂽ��ł��B�ܘ_�A�����̑��ɂ��A���ғ����𖾂�i�߂Ă���r���́A�]�E���g�̂��傫�����Ɋ��ɂȂ�Ȃ��@�\���܂����݂���̂ł��傤�B �@��^�b���ǂ����Ċ��ɂȂ�Ȃ��̂��A���̋@���̉𖾂�ʂ��ē���ꂽ�m�������ɁA�]�E�قǑ傫���͂Ȃ����� �|�q�g�������ł����| ���A���ɜ��Ȃ��A�����͏o���Ă��܂�������}����ׂ̉���I�Ȏ��Ö@�̊J���Ɍq����Ǝv���܂��B�A���A�{�_���� ���ُ킪�N�����c�m�`�����̍זE�̒��ɂ����`�q���֒m���čזE�������镨�������o���� �Ƃ̌������e�ł��̂ŁA�o���Ă��܂������זE���O����I�ю��j��b�ł͂���܂���B�l�Ԃ̊����ÂŃE�C���X�ɂs�o�T�R��g�ݍ��݁A���זE����肢���@�ł��̃E�C���X�Ɋ��������A�s�o�T�R�����Ċ��זE��j����@���͍�����Ă��܂����A�]�E�ł̍���̌������ʂ����ɁA�q�g�̂k�h�e�U�����̈�`�q�ڑg�ݍ��ޕ��@���o�ė����̂��Ɖ@���͎v���܂��B���̗l�Ȏ�@�Ŋ��זE��I��I�ɔj�� elegant �Ȏ��Ö@���m�������A�m�[�x���܂���܂���\���͏\�����肻�����Ƃ������܂��B |
||
 |
 |
https://youtu.be/-X5cD6jd914
Mbuti Pygmies of the Rainforest�@Michael Skinner�@2017/08/29 �Ɍ��J
A classic (old) documentary which looks at the traditional lifestyle of a hunter gatherer
society - the Mbuti Pygmies. Deep in the Itiri Rainforest (Congo), Sangoo and his fellow
villagers live a life untouched by outside influences - a life as close to the earliest
humans as possible.
�U�C�[���̔M�щJ�тɌǗ����ĕ�炷���u�e�B�s�O�~�[�B�@���Ƃ��Ă͔M�щJ�тɐ�������
�}���W�J�ƃI�J�s�̎p�����邱�Ƃ��ł��A��ϋ����[�������ł��B�]�E��|�����̂��F���x��
�Ȃ��犽��̐��������܂����A�������������Ɠ��̔��������܂��B����̓s�O�~�[�̃|���t�H
�j�[�Ƃ��Ēm������̂ł����A�@���͂b�c�����͎����Ă��܂����A�f���Ŋm�F�o���Ċ���
�ł����B����������ɂ��Ă���̏W�����͑�ς����ł��ˁB
 |
 |
|
�@���̘_���́A�ł͂Ȃ��]�E�͑傫���Ȃ�����ɐi�������̂��A���̍�����₤�d���ł͂���܂���B�������X�N��}���ē������傫���Ȃ鎖�����e����O������ɂ��Ēm����^����d���ł��B�������g�̂̃T�C�Y���^������������ɐi������Ӌ` �i�傫���Ȃ�ƃg�N������H�j �ɂ��ẮA�ʂ̍��ŏڂ����G�ꂽ���Ǝv���܂��B�����̃{�f�B�T�C�Y�̑�^���ɔ����A�`�Ԃ̃v���|�[�V�����A�����A�s�����ω����鎖�ɂ��ẮA�R�����̋t�����̍��ɂăA�����g���[�̊T�O�ŐG��܂������A���x�̓T�C�Y��ω�������i���K�����̂��̂��l���悤�Ƃ̘b�ɂȂ�܂��B�ȑO�ɑ�w�ōu�`�������e�����t���b�V�����Ď��M�ł���ƍl���Ă��܂��B �@���̘_���̖`���ŁA�������ɉ����ẮA�g�̂̃T�C�Y�̑傫���̂قNJ��ɜ늳���₷���Ƃ̐�s���������p����Ă���A�C�k�ł��l�Ԃł����̎��������炩�ɂ���Ă���Ƃ̋L�q������A�����[���v���܂����BPeto �̃p���h�b�N�X�͕ʎ퓯�m���r�����ꍇ�̘b�ł����A����Ƃ͈قȂ�A����ł̘b�ƂȂ�܂��B�������ł́A�g�̂��傫����Ί��̉�̔������������܂����A1�P�̍זE�ɂ͓��� �s�o�T�R �̐����������Ȃ���ł�����A�����ׂ��̂�����ςɂȂ����Ƃ͂܂������͂ł��܂��ˁB�ƂȂ�ƃA�t���J�̃W�����O���ɏZ��ł���s�O�~�[�͊����̜̂늳���͒Ⴂ�̂�������܂���B �@�����ɑ��铮���̃{�f�B�T�C�Y������K���헪���𖾂��邱�Ƃ͂Ȃ��Ȃ������[�����ł��ˁB����������Ɖ�X�́u���ɜ늳����v���Ƃ̓N�w���A�����āu������v���Ƃ̓N�w���A���������ς܂ł����[�߂Ă���邩������܂���B |
||
 |
 |


